شرح حالات المادة
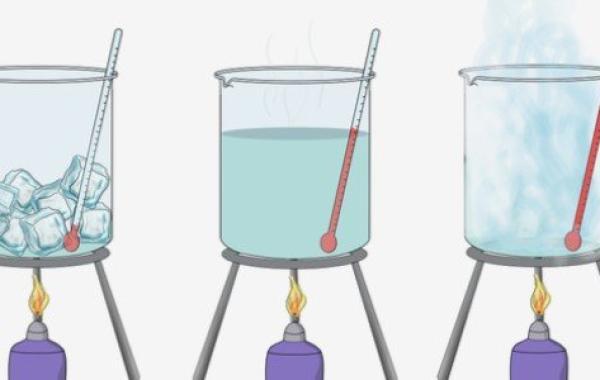
شرح حالات المادة
تتواجد المادة بالطبيعة بواحدة من 3 حالات، وهي الحالة الصلبة، أو الحالة السائلة، أو الحالة الغازية، ويمكن للمادة أن تنتقل من حالة إلى أخرى فالمواد الصلبة بمكن أن تنصهر فتصبح سائلة، والمواد السائلة يمكن أن تتبخر فتصبح غازية، أو العكس فالمواد السائلة قد تتجمد وتصبح صلبة، وهكذا، وفي هذا المقال سنوضح حالات المادة الثلاث.
الحالة الصلبة
هي حالة من حالات المادة الثلاث، والتي تتميز بخصائص معينة تميزها عن السوائل والغازات، على سبيل المثال، لدى الحالة الصلبة القدرة على مقاومة أيّ قوة تُطبق على سطحها، كما أنّ الحالة الصلبة للمركبات تعتمد إلى حدٍ كبير على خصائص الذرات مثل القوى التي تعمل فيما بينها وكيفية ترتيبها.
أبرز خصائص الحالة الصلبة
تمتلك المواد الصلبة خصائص فيزيائية وكيميائية، أبرزها ما يأتي:
- تكون المواد الصلبة غير قابلة للضغط، ممّا يعني أن الجسيمات المكونة مرتبة بالقرب من بعضها البعض، وبسبب ذلك هناك مساحة ضئيلة بين مكونات الجسيم المكون.
- تكون هذه المادة صلبة جدًا، وذلك بسبب عدم وجود مسافة بين الذرات المكونة لها مما يجعلها صلبة ومتماسكة مع بعضها البعض.
- تتمتع المواد الصلبة بأنّ لها كتلة وحجم وشكل محدد، وذلك بسبب تراص الجسيمات المكونة لها.
- تُعد المسافة بين ذرات الحالة الصلبة قصيرة، وينتج عن ذلك قوة قوية جدًا بين الجسيمات المكونة لها.
- يُمكن لجزيئات المواد الصلبة أن تتحرك فقط حول مواضعها المتوسطة.
- لدى المواد الصلبة انضغاطية ضئيلة بسبب المسافة الضئيلة بين الجزيئات المجاورة.
- لدى المواد الصلبة ميل للحفاظ على شكلها عند تعرضها لقوة خارجية.
- تتميز المواد الصلبة بأنّها تقوم باسترجاع شكلها وحجمها الأصلي عند رفع قوة خارجية عنها، وهذا ما يُسمى بخاصية المرونة.
- تتميز المواد الصلبة بحاجتها لدرجة حرارة عالية من أجل تعريضها للانصهار.
- تتميز المادة الصلبة بأسلوب تحولها إلى الحالة الغازية دون مرورها بالحالة السائلة، وهذا ما يُعرف ب خاصية التسامي .
- تتميز الحالة الصلبة بانتقالها إلى الحالة السائلة عند تعريضها لدرجات حرارة مرتفعة، وهذا ما يُعرف بخاصية الذوبان.
أمثلة على مواد بالحالة الصلبة
تتعدد الأمثلة عن المواد بالحالة الصلبة، ومن أبرز هذه الأمثلة ما يأتي:
- الكوارتز (SiO2).
- الماس.
- الجليد.
- كلوريد الصوديوم (NaCl) والذي يُعرف أيضًا باسم ملح الطعام.
الحالة السائلة
تُعد الحالة السائلة للمادة مرحلة وسطية بين الحالة الصلبة والحالة الغازية، حيث أنّ قوى التجاذب بين جزيئات المواد السائلة والتي تفصل بينها مسافات كبيرة؛ تجعل منها جزيئات غير ثابتة في مكانها ومائلة أكثر للحركة، ويُساعد التجاذب بين هذه الجزيئات على بقاء حجم السائل ثابتًا.
أبرز خصائص الحالة السائلة
تعد الحالة السائلة في الفيزياء أحد الحالات الثلاثة للمادة، حيث تُعد الوسيط بين الحالة الصلبة والحالة الغازية، وتتميز بعدة خصائص منها ما يأتي:
- لا يوجد لها شكل محدد؛ حيث تأخذ شكل الوعاء الموضوعة فيه.
- لها حجم محدد.
- الجسيمات لديها حرية التحرك فوق بعضها البعض، لكنها تملك قوى تجاذب فيما بينها.
- تتمتع ب خاصية التوتر السطحي .
- تتمتع بخاصية التماسك والتلاصق.
- تتدفق الحالة السائلة من مرحلة إلى أخرى.
- تحتوي السوائل على درجات غليان أعلى من درجة حرارة الغرفة، وذلك وفقًا الظروف العادية.
- تمتلك المواد السائلة القدرة على نقل الموجات الصوتية في الوسط بسرعة تصل إلى 1 كم في الثانية.
أمثلة على مواد بالحالة السائلة
يوجد العديد من الأمثلة المواد السائلة، وهي كما يأتي:
- معدن الزئبق الموجود في ميزان الحرارة.
- المشروبات.
- مياه البحر.
الحالة الغازية
يُعتبر الغاز أحد حالات المادة التي ليس لها شكل وحجم ثابت، وذات كثافة منخفضة مقارنًة بحالات المادة الأخرى، ويعود السبب في امتلاك جزيئات الغاز طاقة حركية عالية؛ إلى وجود مسافة كبيرة بين جزيئاتها حيث تتصادم فيما بينها ممّا يؤدي إلى سرعة انتشارها في الوعاء، وتوزيعها بشكل متساوي.
ومن الجدير بالذكر أنّ سرعة انتشار جزيئات الغاز مرتبطة بدرجة الحرارة بعلاقة عكسية.
أبرز خصائص الحالة الغازية
وهي المواد التي تمتلك جسيمات متباعدة عن بعضها البعض وسريعة الانتشار، حيث تمتلك خصائص عدة منها ما يأتي:
- لا يوجد لها شكل محدد؛ حيث تأخذ شكل الوعاء الموجودة فيه.
- لا يوجد لها حجم محدد.
- تتحرك الجسيمات في حركة عشوائية، حيث أن قوى التجاذب فيما بينها قليلة أو منعدمة.
- شديدة الانضغاط.
- تختلط الغازات في جميع النسب بدون أيّ وسط ميكانيكي.
- تُمارس الغازات الضغط بالتساوي وفي كافة الاتجاهات.
- تتميز الحالة الغازية بتحولها إلى الحالة الصلبة دون المرور بالحالة السائلة، وهذا ما يُعرف بخاصية الترسيب.
أمثلة على مواد بالحالة الغازية
يُوجد العديد من الأمثلة على المواد بالحالة الغازية في محيطنا، وهي كما يأتي:
- الهواء المحيط بنا.
- غاز الأكسجين.
- غاز الهيليوم .
- غاز الهيدروجين.
- غاز النتروجين.
حالة البلازما
تُعد البلازما حالة من حالات المادة التي يُعتقد بأنّها مجموعة فرعية من الغازات، لكن تختلف بصفاتها عنها، ويُشار إلى أنّ البلازما بأنها ليست حالة شائعة للمادة على الأرض، لكنها قد تكون أكثر شيوعًا في الكون، كما تتكون البلازما من جسيمات مشحونة للغاية مع طاقة حركية مرتفعة جدًا.
أبرز خصائص حالة البلازما
من أبرز خصائص حالة البلازما التي تميزها عن غيرها من حالات المواد، ما يأتي:
- تُعد البلازما حالة ليس لها حجم أو شكل ثابت.
- تُعد كثافة البلازما أقل من المواد الصلبة أو السوائل.
- تتكون البلازما من ذرات تم تجريد بعض أو كل إلكتروناتها، وتتجول فيها نوى موجبة الشحنة بحرية وهي تُسمى الأيونات، وذلك على عكس الغازات العادية.
- تُوجد البروتونات والإلكترونات بداخلها بأعداد متساوية، مما يجعلها متعادلة كهربائيًا.
- تُستخدم البلازما الحرارية لتعقيم المنتجات الغذائية الطازجة؛ نظرًا لقدرتها على قتل البكتيريا.
- يُمكن تثبيت البلازما في مكانها بواسطة الحقول المغناطيسية.
- تستخدم حالة البلازما الغازات النبيلة لتكوينها وتأينها، وذلك لعمل إشارات مشعة باستخدام الكهرباء، ومن الأمثلة عن الغازات النبيلة النيون، والأرجون، والكريبتون، والزينون، والرادون، وغيرها.
أمثلة على مواد بحالة البلازما
تُوجد العديد من الأمثلة على مواد بحالة البلازما، وهي كما يأتي:
- النيتروجين (N).
- كبريتيد الهيدروجين (H 2 S).
- موجات ألفين (Alfvén wave).
- البلازما في مصباح الفلورسنت أو علامة النيون.
- كرات البلازما المليئة بمزيج من الغازات النبيلة التي تنتج ألوان البرق بداخلها.
- تحدث حالة البلازما في الشفق الذي يحيط منطقة القطبين، وذلك عندما تكون الرياح الشمسية عبارة عن تيارات من الجسيمات المشحونة (أيّ تتكون معظمها من البروتونات).
حالة تكاثف بوز-أينشتاين
تُعرف بأنّها هي حالة من حالات المادة التي يدمج فيها الذرات المنفصلة أو الجسيمات دون الذرية في كيان ميكانيكي كمي واحد؛ وذلك باستخدام مزيج من الليزر والمغناطيس.
وتمت هذه العملية في عام 1995 م وذلك بتبريد عينة من عنصر الروبيديوم في درجة حرارة تصل إلى ما يقارب الصفر المطلق، أيّ ما يساوي - 273.15 درجة مئوية.
وعند وصول العينة المستخدمة من ذرات الروبيديوم إلى الحرارة المنخفضة، تتوسع موجاتها وتبدأ في التداخل، أيّ أنّ ذراتها تتقارب فتكون قريبة من حالة السكون وهذا بسبب عدم وجود طاقة حركية التي تنتقل الذرات من مكان لآخر، وبعد ذلك تبدأ هذه الذرات في التجمع معًا فت صبح متطابقة مع بعضها البعض، ومنها تتكون ذرة واحدة كبيرة بدلًا العديد من الذرات المنفصلة.
ومن الجدير بالذكر أنه ومنذ عام 2011 م، بدأ العلماء في دراسة الخصائص الغير مكتشفة لمكثفات بوز - آينشتاين، ومنها سيكتشف العلماء العديد من المجالات والاستخدامات التي ستفيد العلم والمجتمعات من خلال التعمق أكثر بدراسة هذه الحالة.